数据完整性在Pharma公司中的问题:EY调查
卢比结束了乐观!连续三个会话贬值连续
强烈的技术在卢比收入。494.81 MN.
太阳能生产需要群众运动:苛刻的火山
六月快乐!sensex,漂亮开始新的系列爆炸
SPICEJET计划扩大舰队:举报
由于许可证取消恐惧,阳光电视台崩溃了26%
长春市2021年中考中高职贯通培养录取结果、征集计划和志愿发布
今日热榜丨省气象台继续发布高温蓝色预警信号
英学者:美国编造谎言 政治化新冠疫情溯源和世卫组织
路透社报道侯志慧夺金配图阴损,中国使馆发推驳斥:别管自己叫公正媒体了,无耻!
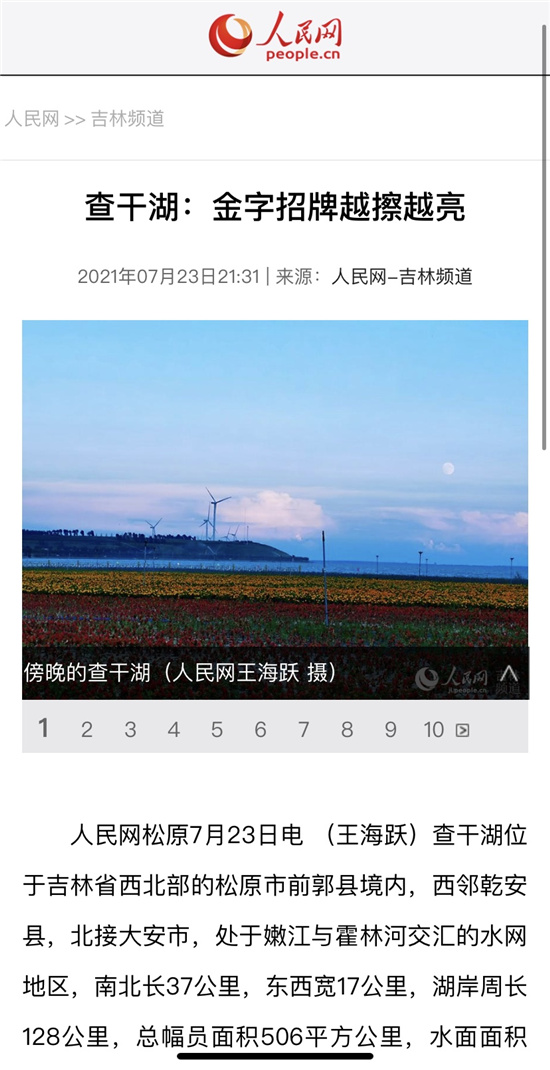
建党百年庆华诞 振兴发展看吉林丨特别观察:河湖连通带来了幸福生活
“黑土地论坛”发布6条倡议推进黑土地保护
著名体育记者陈涛做客直播间:东京奥运会开幕式,中国代表团入场很惊艳
人民日报钟声:依法反击美方制裁,中方说到做到
暴雨!吉林省连发预警
长影周末音乐会回归 上演“暑期欢乐总动员”
卢伟:从土专家到优秀乡村人才 带动大伙儿增收致富
建党百年庆华诞 振兴发展看吉林丨vlog:这里歌声嘹亮,笑颜如花
2021长春市民换书大集火爆来袭
前方暴雨,火车为什么要停运?
我身边的党员故事|(93)情系福利院、爱在行动中的刘凤梅
我身边的党员故事|(91)长春市外办党总支:感动!来自德国专家的一封感谢信
建党百年庆华诞 振兴发展看吉林丨一路走,一路拍 看见“不一样”的吉林
基本事实与正常逻辑很难吗?
印度被曝用间谍软件监控多国政要 巴基斯坦外交部:呼吁联合国彻查
Sun Pharma在Ranbaxy Integration后3年的旨在为250 MN Synergy提供了250 MN Synergy:Uday Baldota.
飞翔的荷兰人!印度:rain
PNC Infratech从国家高速公路-86的Kanpur-Kabrai部分开始收费运营
啊!Mark Mobius投资熵创新
美国经济增长前景良好,但脆弱性的口袋:Christine Lagarde.
塔塔集团追捕两个职位
尼日利亚是原油的第四最大来源:Dharmendra Pradhan.
KV Kamath下个月承担金砖银行的费用
每日市场战略 - 有些反弹应该发生!
卢比没有看到急剧下降:博士室
Mahavir Inds,VGCL Log Bulk Opds
Sun Pharma在Ranbaxy Integration后3年的旨在为250 MN Synergy提供了250 MN Synergy:Uday Baldota.
再次汤!雀巢印度坍塌9%
印度和欧洲需要合作知识产权:Rajiv Aggarwal.
喷气式飞机在粉红色的滑动滑动到50外国人飞行员:举报
卢比没有看到急剧下降:博士室
美国经济增长前景良好,但脆弱性的口袋:Christine Lagarde.
emami在'kesh king'买断时跳跃2.8%
煤炭印度希望在2016财年以30%维持eBITDA:Bipin Kumar Saxena.
喷气式飞机在粉红色的滑动滑动到50外国人飞行员:举报
Hero Motocorp销量在5月份下降5.4%
塔塔钢铁工人准备无限罢工表示联合
“德尔塔”变异毒株在美肆虐 全美感染和住院病例数上升
美国近90%地区新冠确诊病例数攀升
 根据AU的调查,三分之一的制药公司没有进行审查以评估数据完整性的潜在差距,“印度制药行业的数据完整性符合性”。数据完整性审查进行评估,以评估IFData记录是准确的,完整,归属,清晰的,并在其原始背景下维护电子或纸张形式.PORPS30%的受访者表示,他们已经通过监管机构接受了检验观察。尽管签署了他们的理解和遵守良好的制造实践(GMP)Norms.ARPinder
根据AU的调查,三分之一的制药公司没有进行审查以评估数据完整性的潜在差距,“印度制药行业的数据完整性符合性”。数据完整性审查进行评估,以评估IFData记录是准确的,完整,归属,清晰的,并在其原始背景下维护电子或纸张形式.PORPS30%的受访者表示,他们已经通过监管机构接受了检验观察。尽管签署了他们的理解和遵守良好的制造实践(GMP)Norms.ARPinder Singh,合作伙伴和国家领导者,欺诈调查和争议服务,“制药行业也是国内眼中的浮力部门作为外国投资者。但与此同时,行业仍在努力应对国内市场定价的挑战,增加的法规和数据诚信有关需要认真对待这些问题,特别是数据完整性,因为它是一个关键方面总体合规框架。“”维护数据完
整性对于制药部门至关重要。如今,有现有或预期涉及数据完整性的公司应常规主动数据完整性评估。即使对于在市场上享有良好声誉的公司,这将是有益的。这些定期评估为所有参与的所有利益攸关方提供保证 - 客户,投资者,监管机构以及重申管理层对最高质量标准的承诺。“添加rajiv Joshi,合作伙伴,欺诈调查和争议服务,ey.dr.
Ajaz S. Hussain,Advisor,Ey和前副主任,美国食品和药物管理局(美国FDA)补充说,“数据的诚信是我们对质量,安全性和疗效做出决定的基础。以准确性记录数据和信息保护寿命;没有它,我们不能区分假冒和真实的药物。最后,任何在数据完整性保证的失效都是与预期实践的严重偏差,并且可能会产生不利影响。EY调查是一个APT提醒 - 一种提高意识和传达这一重要信息的手段。“Ey的欺
诈调查和争议服务团队进行了调查,评估了与制药公司面临的数据完整性遵从性有关的合规状况。调查的一些关键亮点是:
技术升级是每小时的需求 - 25%的人不知道美国FDA规定的21码联邦监管(CFR)第11部分标准,该第11部分规定了以电子形式记录数据的标准.33%提到有共同的员工登录ID和密码,用于高效液相色谱(HPLC),气相色谱(GCS)。这表明,组织仍然需要对符合全球标准进行重大进展。重要的是,管理层必须更加关注这些要求,因为未能这样做,可以邀请监管和/或刑事
后果。工人的压力和短缺影响质量遵守 - 超过57%的员工同意已经看到了工作压力制造人员满足关键绩效指标(KPI),如产出量,低拒绝比和整体设备有效性.18%没有充分的人员质量保证团队独立审查所有产品的制造和测试。这表明人力或过度工作压力的短缺可能导致不准确或不完整的文件,最终可能影响产品质量。质量流
程和程序 - 33%的受访者没有进行评估潜在差距,以评估数据完整性的潜在差距。已经观察到,定期和积极的数据完整性评论可以确保GMP数据的准确性和一致性.13%的受访者没有明确记录的标准操作程序(SOP)备份和删除HPLC或GCS.LAPSES生成的实验室数据文件的备份和删除数据
完整性继续上升 - 超过30%的受访者已经接受了诸如表格483s,警告信,进口警报,不遵守GMP等的检验观察结果,并由全球监管机构发布.21%表示审计设备上的审计跟踪是在其组织中并不总是启用。缺乏审计跟踪可能是一个严重的问题,因为没有捕获的数据记录,可能导致监管机构的严重行动。诱
导题外吹口框架,仍在进步 - 28%的受访者表示他们的组织没有欺诈报告机制到位。在这种守卫的行业中,缺乏吹口哨的政策意味着自杀,他真正希望通过标记任何不道德的行为或不列颠战争或不列颠官方来帮助他们的组织可以被迫在外部报告这些问题。
免责声明:本网站所有信息仅供参考,不做交易和服务的根据,如自行使用本网资料发生偏差,本站概不负责,亦不负任何法律责任。涉及到版权或其他问题,请及时联系我们。