SPARC从USFDA获得CRL for Latanoprost NDA
Gateway Distriparks在Krishnapatnam港口建立集装箱货运站
台商担忧共同富裕是吃“大锅饭”? 国台办:绝不是“劫富济贫”
扬州地区火车站15日12时起恢复售票
吃大蒜、喝绿茶、用特定牙膏刷牙……消灭胃中“幽灵”,这些网传招数都不靠谱
中国代表在人权理事会对日本核污染水排海问题表达严重关切
新华国际时评:五个“率先”彰显推动抗疫合作的中国担当
锐参考 | 被捧为“印太沙皇”的他,居然使出这种“昏招”——
身高焦虑就打增高针?小心打出健康问题
北京今年以来降雨形成水资源量46.28亿立方米
国际观察:美国抗疫大溃败的五个“病根”
债券“南向通”上线在即 金融市场双向开放再进一步
美国儿童新冠肺炎病例呈上升趋势
专访:科兴疫苗因安全、有效获准紧急使用于少年儿童——访智利公共卫生研究院代院长加西亚
福建省加强保障疫情防控期间应急物资正常流通
美媒:每500名美国人就有1人死于新冠 儿童确诊病例持续激增
市场监管总局发布2021年月饼专项抽检不合格情况通告
关注丨长春盛北大街与新开大街何时能贯通?官方最新回应来了
农业资源循环创新利用 安图县打造杏鲍菇产业生态发展之路
厦门累计报告新冠肺炎确诊病例48例
5种门诊慢特病将试点跨省直接结算
人工关节 为何降价超八成
联合国贸发会议:中国经济表现突出 在进出口领域更早复苏
“新时代新征程 媒眼‘看’安图”全国重点新闻媒体采访活动启动
首部农业绿色发展专项规划出台
你家的摄像头在盯着你!不法分子侵入家用摄像头案例引关注
多国在人权理事会发言反对外部势力干涉中国内政
大湾区购物节:港澳企业积极推进数字化转型 拓展内地市场
社评:英国驻华大使以后别来人民大会堂了
国际锐评丨中国仍是全球经济增长的“独特支柱”
国台办:坚决反对任何形式的“修宪谋独”行径
莆田数十名儿童感染新冠病毒 如何织密学校疫情防控网
债券市场“南向通”将于9月24日上线
8月份国民经济发展韧性持续显现
三部门要求健全残疾人两项补贴标准动态调整机制
部分景区票价偏高 发改委开展“回头看”
未成年人网游这条生意链怎么断
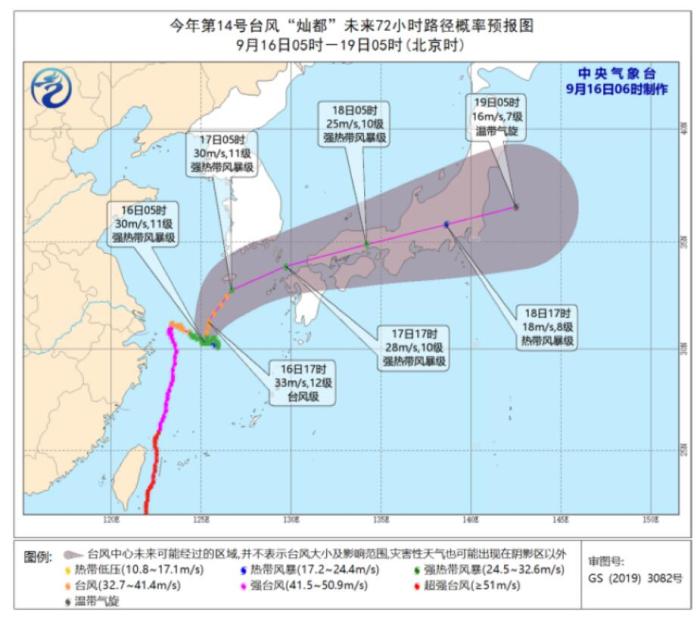
四川盆地等地仍有较强降水 “灿都”继续影响东海等海域
吉林省卫生健康委关于新型冠状病毒肺炎疫情情况通报(2021年9月16日公布)
赵立坚现场展示漫画 三问美国保护的是什么人权?
贝尔觉醒世预赛戴帽 博鱼sports携手红龙冲击世界杯
贝尔觉醒世预赛戴帽 博鱼sports携手红龙冲击世界杯
LS扬声器暂停25个国会成员的不当行为
HDFC计划提高新资本的计划
法拉隆,黑石在Rccom Tower股权的比赛中
Gateway Distriparks在Krishnapatnam港口建立集装箱货运站
Vardhman Textiles Hits 52周高
vipul jain辞去了Accelya Kale的MD; Neela Bhattacherjee成功
Bharti Airtel计划于12月加入1,000家商店
飞高!Spicejet Q1 Q1净利润为71.8卢比,工业负载系数最高
 Sun Pharma Advanced Research Company Ltd.(SPARC)宣布美国食品和药物管理局(USFDA)已向其新药物申请(NDA)发布了一份完整的响应信(CRL),为Xelpros,Latanoprost Bak-Free EyeDrops.sparc提
Sun Pharma Advanced Research Company Ltd.(SPARC)宣布美国食品和药物管理局(USFDA)已向其新药物申请(NDA)发布了一份完整的响应信(CRL),为Xelpros,Latanoprost Bak-Free EyeDrops.sparc提交了a对其从USFDA接收的早期CRL的响应,其中不需要额外的临床前或临床数据。虽然USFDA已接受澄清和对标签的变化,但SPARC现在已经从USFDA获得了另一种CRL,寻求对拟议标签的微小变化。SPARC希望很快就希望解
决这些要求。这产品将在SPIL的HALOL设施制造,USFDA表明,此设施的CGMP缺陷令人满意的解决是XelPROS最终批准的先决条件。SPARC最近向Sun Pharmaceutical Industries Ltd(SPIL)的子公司提供了许可。
免责声明:本网站所有信息仅供参考,不做交易和服务的根据,如自行使用本网资料发生偏差,本站概不负责,亦不负任何法律责任。涉及到版权或其他问题,请及时联系我们。